Unsere ImmunoSafe-HLA I- und ImmunoSafe-HLA II-Panels wurden sorgfältig entwickelt, um die Vorhersagbarkeit Ihrer präklinischen Assays zu verbessern. Mit 10 HLA-Klasse-I- oder HLA-Klasse-II-kompatiblen Spendern können diese Panels auf Ihre spezifischen Assay-Anforderungen zugeschnitten werden. Durch die Bereitstellung einer umfassenden Ressource zur Nachahmung verschiedener immunologischer Reaktionen ermöglichen sie den Forschern genauere und spezifische Versuchsergebnisse. Ihre Vielseitigkeit und Anpassungsfähigkeit gewährleisten eine nahtlose Integration in bestehende Forschungsprotokolle und machen sie zu unschätzbaren Werkzeugen für die Entschlüsselung der Komplexität des Immunsystems und die Förderung bahnbrechender Entdeckungen in der biomedizinischen Forschung.
| Prospective collection of specific subsets of PBMC* | ||
|---|---|---|
| OFFER NO. | PRODUCT | SPECIFICATION |
| 133 94113 010 | Human PBMC, healthy donor, ImmunoSafe-HLA1 | Cryo, 10 × 106 cells/vial |
| 133 94113 020 | Human PBMC, healthy donor, ImmunoSafe-HLA1 | Cryo, 20 × 106 cells/vial |
| 134 94114 010 | Human PBMC, healthy donor, ImmunoSafe-HLA2 | Cryo, 10 × 106 cells/vial |
| 134 94114 020 | Human PBMC, healthy donor, ImmunoSafe-HLA2 | Cryo, 20 × 106 cells/vial |
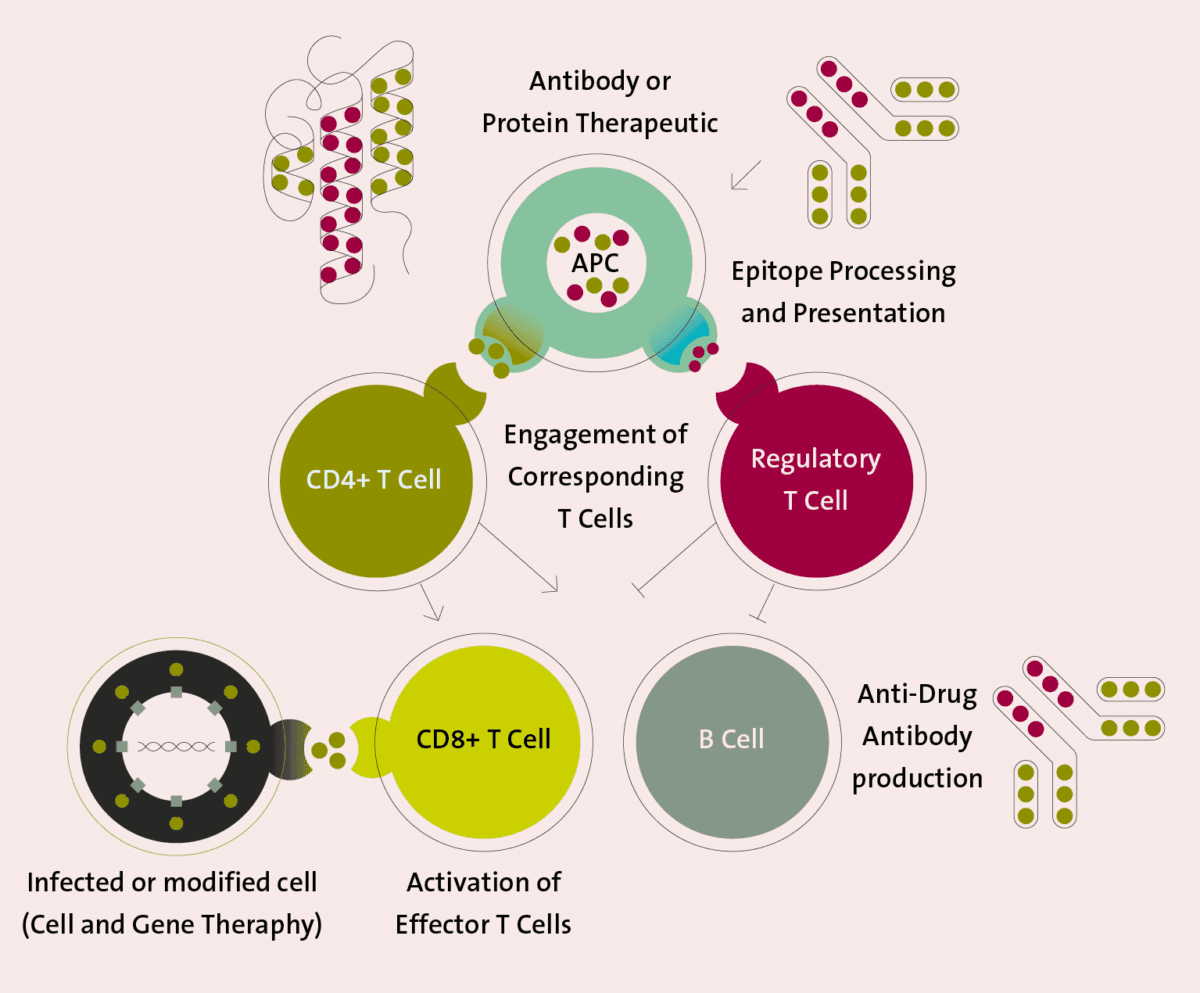
Die Bewertung des Immunogenitätsrisikos neuartiger Proteintherapeutika ist von entscheidender Bedeutung, um ihre Sicherheit und Wirksamkeit zu gewährleisten. Sie ist mit mehreren Herausforderungen verbunden, darunter Schwankungen der Immunantwort zwischen verschiedenen Populationen, die Veränderung der Immunogenität von Impfstoffen mit zunehmendem Alter und die allgemeine Nichteignung von Tiermodellen für die Prognose von Immunantworten beim Menschen.